Apakah Anda pernah mendengar istilah anoda katoda? Dalam dunia teknologi dan elektronika, anoda katoda adalah dua komponen yang sangat penting. Mereka memiliki peran vital dalam berbagai perangkat elektronik modern seperti baterai, lampu neon, tabung sinar katoda, dan banyak lagi. Dalam artikel ini, kami akan menjelaskan secara detail apa itu anoda katoda, bagaimana mereka bekerja, dan contoh penggunaannya dalam kehidupan sehari-hari.
Sebelum kita memahami lebih jauh tentang anoda katoda, mari kita lihat definisi masing-masing. Anoda adalah elektroda positif dalam suatu sistem elektrokimia atau tabung hampa, sedangkan katoda adalah elektroda negatif. Perbedaan polaritas ini penting dalam menghasilkan aliran arus elektron. Anoda dan katoda bekerja bersama-sama untuk menghasilkan reaksi redoks atau emisi elektron, tergantung pada konteks penggunaannya.
Pengertian Anoda dan Katoda
Pada bagian ini, kita akan mendefinisikan secara jelas apa yang dimaksud dengan anoda dan katoda. Kami akan menjelaskan peran masing-masing dalam konteks berbagai perangkat elektronik.
Anoda adalah elektroda positif dalam suatu sistem elektrokimia atau tabung hampa. Dalam konteks baterai, anoda adalah elektroda dimana oksidasi terjadi. Artinya, anoda adalah tempat terjadinya reaksi redoks dimana atom atau molekul kehilangan elektron. Anoda juga berfungsi sebagai titik masuk arus listrik positif ke dalam perangkat elektronik. Contoh anoda adalah elektroda positif dalam baterai, seperti anoda dalam baterai AA yang terbuat dari seng.
Katoda adalah elektroda negatif dalam suatu sistem elektrokimia atau tabung hampa. Dalam konteks baterai, katoda adalah elektroda dimana reduksi terjadi. Artinya, katoda adalah tempat terjadinya reaksi redoks dimana atom atau molekul menerima elektron. Katoda juga berfungsi sebagai titik keluar arus listrik negatif dari perangkat elektronik. Contoh katoda adalah elektroda negatif dalam baterai, seperti katoda dalam baterai AA yang terbuat dari karbon.
Peran Anoda dan Katoda dalam Berbagai Perangkat Elektronik
Anoda dan katoda memiliki peran yang berbeda dalam berbagai perangkat elektronik. Dalam baterai, anoda dan katoda bekerja bersama-sama untuk menghasilkan arus listrik. Anoda adalah tempat terjadinya oksidasi, sedangkan katoda adalah tempat terjadinya reduksi. Ketika baterai digunakan, reaksi redoks terjadi di dalamnya, dimana pada anoda terjadi oksidasi dan pada katoda terjadi reduksi. Perbedaan potensial antara anoda dan katoda memungkinkan aliran elektron dan menghasilkan energi listrik.
Contoh lain penggunaan anoda dan katoda adalah dalam lampu neon. Lampu neon mengandalkan emisi foton dari gas neon untuk menghasilkan cahaya. Ketika arus listrik mengalir melalui gas neon dalam lampu neon, reaksi redoks terjadi di antara anoda dan katoda. Elektron yang dihasilkan dari reaksi redoks ini bertabrakan dengan atom neon, menyebabkan emisi foton dan menghasilkan cahaya neon yang terkenal.
Tabung sinar katoda adalah perangkat elektronik lain yang menggunakan anoda dan katoda. Dalam tabung sinar katoda, katoda menghasilkan aliran elektron dengan pemanasan termal atau medan listrik. Elektron ini dipercepat menuju anoda dan dengan demikian menghasilkan sinar elektron. Tabung sinar katoda banyak digunakan dalam televisi tabung, monitor komputer, dan perangkat elektronik lainnya yang membutuhkan pemancaran elektron.
Bagaimana Anoda dan Katoda Bekerja?
Dalam bagian ini, kita akan menjelaskan bagaimana anoda dan katoda bekerja secara teknis. Kami akan membahas proses aliran arus listrik dan reaksi kimia yang terjadi di dalamnya.
Saat anoda dan katoda terhubung dalam suatu rangkaian, perbedaan potensial antara keduanya menciptakan medan listrik. Medan listrik ini mendorong elektron untuk bergerak dari katoda ke anoda. Elektron-elektron ini membawa muatan negatif dan oleh karena itu menghasilkan arus listrik. Proses ini disebut dengan aliran arus listrik atau konduksi elektron.
Reaksi kimia juga terjadi di antara anoda dan katoda. Pada anoda, reaksi oksidasi terjadi dimana atom atau molekul kehilangan elektron. Hal ini memungkinkan anoda menjadi tempat terjadinya oksidasi. Pada katoda, reaksi reduksi terjadi dimana atom atau molekul menerima elektron. Hal ini memungkinkan katoda menjadi tempat terjadinya reduksi. Dalam beberapa kasus, reaksi redoks di antara anoda dan katoda menghasilkan emisi elektron atau pemancaran sinar elektron.
Fungsi Anoda dan Katoda dalam Baterai
Dalam bagian ini, kami akan mengulas peran anoda dan katoda dalam baterai. Kami akan menjelaskan bagaimana mereka berinteraksi dengan elektrolit dan bagaimana hal ini memungkinkan baterai menyimpan dan melepaskan energi.
Anoda dalam baterai adalah tempat terjadinya oksidasi. Ketika baterai digunakan, reaksi kimia di anoda menghasilkan elektron dan ion. Elektron-elektron ini mengalir melalui rangkaian eksternal, menghasilkan arus listrik. Ion-ion yang dihasilkan dari reaksi redoks di anoda bergerak melalui elektrolit menuju katoda.
Katoda dalam baterai adalah tempat terjadinya reduksi. Ion-ion yang bergerak melalui elektrolit dari anoda menuju katoda merespons elektron-elektron yang mengalir melalui rangkaian eksternal. Proses ini menghasilkan emisi elektron di katoda dan menghasilkan reaksi redoks di katoda. Reaksi redoks ini memungkinkan katoda menjadi tempat terjadinya reduksi.
Perbedaan potensial antara anoda dan katoda dalam baterai memungkinkan aliran elektron dan menghasilkan energi listrik. Ketika baterai digunakan dan arus listrik mengalir melalui rangkaian eksternal, reaksi redoks terus berlangsung di antara anoda dan katoda sehingga baterai dapat menyimpan dan melepaskan energi.
Anoda Katoda dalam Lampu Neon
Lampu neon adalah salah satu contoh perangkat yang menggunakan anoda dan katoda. Dalam bagian ini, kami akan menjelaskan peran mereka dalam menghasilkan cahaya dalam lampu neon.
Lampu neon terdiri dari tabung kaca yang diisi dengan gas neon. Di dalam tabung, terdapat elektroda yang terhubung ke sumber listrik. Salah satu elektroda adalah anoda, sedangkan yang lainnya adalah katoda. Ketika arus listrik mengalir melalui gas neon di antara anoda dan katoda, reaksi redoks terjadi.
Pada anoda, terjadi oksidasi dimana atom atau molekul kehilangan elektron. Proses ini menghasilkan ion-ion positif yang bergerak menuju katoda melalui gas neon. Pada katoda, terjadi reduksi dimana ion-ion positif dari anoda menerima elektron. Elektron-elektron ini bertabrakan dengan atom neon, menyebabkan emisi foton dan menghasilkan cahaya neon yang terkenal.
Anoda Katoda dalam Tabung Sinar Katoda
Tabung sinar katoda adalah perangkat elektronik yang menggunakan anoda dan katoda untuk menghasilkan sinar elektron. Kami akan menjelaskan bagaimana mereka bekerja dan berbagai aplikasi tabung sinar kat
Tabung Sinar Katoda dalam Elektronika
Tabung sinar katoda adalah salah satu perangkat elektronik penting dalam dunia elektronika. Dalam tabung sinar katoda, katoda memancarkan sinar elektron yang dipercepat menuju anoda. Proses ini memungkinkan kontrol arus elektron dan digunakan dalam berbagai aplikasi elektronika seperti televisi tabung, monitor komputer, dan perangkat pemancar sinyal.
Anoda dalam tabung sinar katoda berperan sebagai penarik elektron. Ketika tegangan diberikan ke tabung sinar katoda, katoda dipanaskan hingga mencapai suhu yang cukup tinggi. Panas ini menyebabkan pelepasan elektron dari permukaan katoda. Medan listrik yang dihasilkan oleh anoda kemudian mempercepat elektron-elektron ini menuju permukaan anoda.
Proses ini menghasilkan sinar elektron yang dapat digunakan dalam aplikasi elektronika. Misalnya, dalam televisi tabung, sinar elektron yang dipancarkan oleh tabung sinar katoda mengenai layar yang dilapisi dengan fosfor. Interaksi sinar elektron dengan fosfor menghasilkan cahaya yang kita lihat sebagai gambar di layar televisi.
Contoh Penggunaan Anoda dan Katoda dalam Elektrolisis
Elektrolisis adalah proses kimia yang menggunakan arus listrik untuk memisahkan senyawa menjadi elemen yang terpisah. Dalam elektrolisis, anoda dan katoda berperan penting dalam reaksi redoks yang terjadi.
Contoh penggunaan anoda dan katoda dalam elektrolisis adalah elektrolisis air. Dalam elektrolisis air, air (H2O) dipecah menjadi hidrogen (H2) dan oksigen (O2) menggunakan arus listrik. Anoda dalam elektrolisis air berperan sebagai tempat terjadinya oksidasi air. Pada anoda, air melepaskan elektron dan berubah menjadi oksigen (O2). Elektron-elektron ini mengalir melalui rangkaian eksternal menuju katoda.
Katoda dalam elektrolisis air berperan sebagai tempat terjadinya reduksi air. Pada katoda, elektron-elektron yang mengalir menuju katoda bertemu dengan ion hidrogen (H+) yang berasal dari air. Elektron-elektron ini menyatukan dengan ion hidrogen dan membentuk hidrogen (H2). Dengan demikian, elektrolisis air menghasilkan oksigen di anoda dan hidrogen di katoda.
Perbedaan Antara Anoda dan Katoda
Walaupun anoda dan katoda memiliki peran yang berbeda, ada beberapa perbedaan lainnya yang perlu kita ketahui. Dalam bagian ini, kami akan membandingkan anoda dan katoda dari berbagai segi.
Satu perbedaan utama antara anoda dan katoda adalah polaritasnya. Anoda memiliki polaritas positif, sedangkan katoda memiliki polaritas negatif. Hal ini berarti bahwa arus listrik mengalir dari anoda ke katoda. Dalam konteks baterai, arus listrik mengalir dari anoda melalui rangkaian eksternal ke katoda.
Perbedaan lainnya adalah peran dalam reaksi redoks. Anoda adalah tempat terjadinya oksidasi, sedangkan katoda adalah tempat terjadinya reduksi. Dalam reaksi redoks, atom atau molekul di anoda kehilangan elektron sedangkan atom atau molekul di katoda menerima elektron.
Selain itu, perbedaan lainnya adalah material yang digunakan. Anoda umumnya terbuat dari logam atau paduan logam yang tahan terhadap oksidasi, seperti seng atau timah. Di sisi lain, katoda sering kali terbuat dari material yang mampu menerima elektron dengan baik, seperti karbon atau logam mulia seperti emas atau perak.
Perbedaan Antara Anoda dan Katoda dalam Elektronika
Dalam konteks elektronika, ada perbedaan penting antara anoda dan katoda. Kami akan menjelaskan perbedaan ini dan bagaimana hal itu mempengaruhi cara kerja perangkat elektronik.
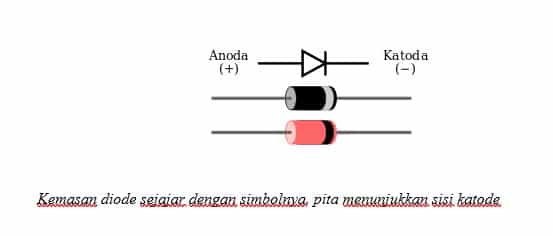
Salah satu perbedaan utama adalah arah aliran arus listrik. Dalam dioda, arus hanya mengalir dari anoda ke katoda, tidak sebaliknya. Dioda adalah komponen elektronik yang hanya memungkinkan arus listrik mengalir dalam satu arah. Hal ini disebabkan oleh polaritas anoda dan katoda yang berbeda dalam dioda. Ketika tegangan diberikan dalam arah yang benar, arus listrik dapat mengalir melalui dioda dari anoda ke katoda. Namun, jika tegangan diberikan dalam arah yang salah, dioda akan menghambat aliran arus.
Perbedaan lainnya adalah peran dalam perangkat elektronik. Anoda sering kali berfungsi sebagai penarik elektron atau sumber arus positif, sedangkan katoda berfungsi sebagai penarik elektron atau sumber arus negatif. Misalnya, dalam lampu neon, arus listrik mengalir dari anoda ke katoda melalui gas neon, menyebabkan emisi foton dan menghasilkan cahaya neon.
Anoda dan Katoda dalam Sel Elektrokimia
Sel elektrokimia adalah perangkat yang menggunakan reaksi redoks untuk menghasilkan listrik. Dalam bagian ini, kami akan menjelaskan peran anoda dan katoda dalam sel elektrokimia dan bagaimana hal itu memungkinkan aliran arus listrik.
Anoda dalam sel elektrokimia adalah tempat terjadinya oksidasi. Pada anoda, reaksi oksidasi terjadi dimana atom atau molekul kehilangan elektron. Hal ini memungkinkan anoda menjadi tempat terjadinya oksidasi dalam sel elektrokimia.
Katoda dalam sel elektrokimia adalah tempat terjadinya reduksi. Pada katoda, reaksi reduksi terjadi dimana atom atau molekul menerima elektron. Hal ini memungkinkan katoda menjadi tempat terjadinya reduksi dalam sel elektrokimia.
Perbedaan potensial antara anoda dan katoda dalam sel elektrokimia memungkinkan aliran arus listrik. Ketika sel elektrokimia digunakan, reaksi redoks terus berlangsung di antara anoda dan katoda sehingga sel elektrokimia dapat menghasilkan listrik.
Contoh Lain Penggunaan Anoda dan Katoda
Selain dalam baterai, lampu neon, dan tabung sinar katoda, anoda dan katoda juga digunakan dalam berbagai perangkat dan aplikasi lainnya. Kami akan memberikan beberapa contoh penggunaan anoda dan katoda dalam kehidupan sehari-hari.
Contoh penggunaan anoda dan katoda lainnya adalah dalam proses elektrolisis dalam pembuatan logam. Dalam proses elektrolisis ini, anoda dan katoda digunakan untuk memisahkan logam dari senyawa logamnya. Anoda terbuat dari logam yang akan dielektrolisis, sedangkan katoda terbuat dari logam murni yang akan didepositkan. Ketika arus listrik diberikan, logam pada anoda teroksidasi menjadi ion logam, sedangkan ion-logam ini bermigrasi menuju katoda dan didepositkan sebagai logam murni.
Contoh lain penggunaan anoda dan katoda adalah dalam pengolahan air limbah. Dalam proses elektrolisis air limbah, anoda dan katoda digunakan untuk menghilangkan polutan dan mengubah senyawa organik menjadi senyawa yang lebih sederhana. Anoda terbuat dari material yang tahan terhadap korosi, seperti titanium, sedangkan katoda terbuat dari material yang reaktif terhadap senyawa organik.
Dalam kesimpulan, anoda katoda adalah dua komponen yang sangat penting dalam teknologi dan elektronika. Mereka memiliki peran yang berbeda tetapi saling melengkapi. Anoda adalah elektroda positif, sedangkan katoda adalah elektroda negatif. Mereka bekerja bersama-sama untukmenghasilkan aliran arus listrik, reaksi redoks, emisi elektron, dan berbagai fenomena lainnya. Dalam berbagai perangkat elektronik dan proses kimia, anoda dan katoda memiliki peran vital.
Anoda berfungsi sebagai tempat terjadinya oksidasi, di mana atom atau molekul kehilangan elektron. Anoda juga bertindak sebagai sumber arus positif dalam perangkat elektronik. Contohnya, dalam baterai, anoda adalah tempat terjadinya reaksi oksidasi yang menghasilkan elektron. Elektron ini kemudian mengalir melalui rangkaian eksternal, menghasilkan arus listrik.
Di sisi lain, katoda berfungsi sebagai tempat terjadinya reduksi, di mana atom atau molekul menerima elektron. Katoda juga bertindak sebagai sumber arus negatif dalam perangkat elektronik. Contohnya, dalam baterai, katoda adalah tempat terjadinya reaksi reduksi yang melibatkan penerimaan elektron. Katoda menerima elektron dari rangkaian eksternal, menghasilkan aliran arus listrik.
Perbedaan polaritas antara anoda dan katoda sangat penting dalam aliran arus listrik. Arus listrik selalu mengalir dari anoda ke katoda, karena arus listrik mengikuti jalur dengan beda potensial yang lebih tinggi ke beda potensial yang lebih rendah. Dalam perangkat elektronik seperti dioda, arus hanya mengalir dalam satu arah, yaitu dari anoda ke katoda.
Selain perbedaan polaritas, anoda dan katoda juga memiliki peran yang berbeda dalam reaksi redoks. Anoda adalah tempat terjadinya oksidasi, di mana terjadi kehilangan elektron. Katoda adalah tempat terjadinya reduksi, di mana terjadi penerimaan elektron. Reaksi redoks yang terjadi di antara anoda dan katoda memungkinkan perubahan kimia dan aliran arus listrik.
Dalam baterai, anoda dan katoda bekerja bersama-sama untuk menghasilkan energi listrik. Anoda berperan dalam reaksi oksidasi, di mana senyawa di anoda teroksidasi dan menghasilkan elektron. Elektron ini kemudian mengalir melalui rangkaian eksternal ke katoda. Di katoda, reaksi reduksi terjadi, di mana senyawa di katoda menerima elektron dan mengembalikan keseimbangan muatan. Proses ini menghasilkan aliran arus listrik dan energi yang dapat digunakan untuk berbagai aplikasi.
Selain dalam baterai, anoda dan katoda juga digunakan dalam berbagai perangkat elektronik lainnya. Misalnya, dalam lampu neon, arus listrik mengalir melalui gas neon antara anoda dan katoda. Reaksi redoks yang terjadi menyebabkan emisi foton, menghasilkan cahaya neon yang terkenal. Dalam tabung sinar katoda, katoda menghasilkan aliran elektron yang dipercepat menuju anoda, menghasilkan sinar elektron yang digunakan dalam aplikasi elektronika.
Dalam proses elektrolisis, anoda dan katoda juga memiliki peran penting. Elektrolisis adalah proses kimia di mana senyawa dipecah menjadi elemen yang terpisah menggunakan arus listrik. Anoda berperan sebagai tempat terjadinya oksidasi, sedangkan katoda berperan sebagai tempat terjadinya reduksi. Misalnya, dalam elektrolisis air, anoda adalah tempat terjadinya oksidasi air menjadi oksigen, sedangkan katoda adalah tempat terjadinya reduksi air menjadi hidrogen.
Dalam kesimpulan, anoda dan katoda adalah dua komponen penting dalam teknologi dan elektronika. Anoda adalah elektroda positif yang berperan dalam reaksi oksidasi, sedangkan katoda adalah elektroda negatif yang berperan dalam reaksi reduksi. Mereka bekerja bersama-sama untuk menghasilkan aliran arus listrik, reaksi redoks, dan berbagai fenomena lainnya dalam perangkat elektronik dan proses kimia. Dengan pemahaman yang baik tentang anoda dan katoda, kita dapat lebih menghargai dan memahami berbagai aplikasi teknologi yang ada di sekitar kita.
